Innehåll
Natriumacetattrihydrat är en vanlig och billig förening som används för olika applikationer i livsmedel, industrier och laboratorier. Den används vid betning, garvning, som buffert och som en huvudkomponent i elektriska kompresser. Natriumacetat studeras för användning vid denitrifiering av avloppsvatten som en komponent i nematicider.
Förberedelse
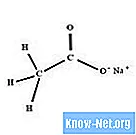
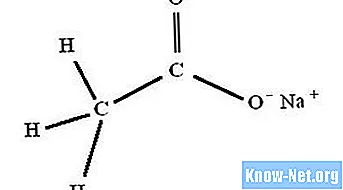
Natriumacetattrihydrat, med den kemiska formeln NaC2H3O2.3H2O, bildas omedelbart genom reaktionen mellan ättiksyra (ättika) och natriumhydroxid, natriumkarbonat eller natriumbikarbonat.
Namn och formel
Det vetenskapliga namnet på ättiksyra är etanol. Av denna anledning kallas natriumacetat ibland natriumetanoat.
Organiska kemister skriver natriumacetatstrukturen som NaC2H3O2.3H2O. I vissa situationer använder de dock den förkortade beteckningen "NaAc".
Matanvändning
I ett en-till-ett-förhållande kan natriumacetat och ättiksyra samkristallisera i en produkt som kallas natriumdiacetat. Denna produkt är mycket användbar i livsmedelsindustrin eftersom den är en nästan luktfri fast substans, men "in situ" bryts den ned i dess komponenter. Både natriumacetat och diacetat har fått GRAS-klassificeringen (från engelska "allmänt erkänd som säker") av Food and Drug Administration.
Natriumacetat används i kött- och fjäderfäindustrin för att förbättra smak. Diacetat används för ett liknande syfte och som en hämmare av tillväxten av patogener.
Medicinsk användning
Natriumacetat i medicin används för att utvinna elektrolyter. Det fungerar också som ett diuretikum.
Den mest intressanta tillämpningen av den är i elektriska kompresser. Natriumacetattrihydrat innehåller tre molekyler kristallvatten. Värm upp till 58 grader Celsius och dessa vatten kommer att frigöras från kristallen. De löser upp det uttorkade natriumacetatet och ersätter det fasta ämnet med en lösning. Denna lösning kan kylas utan omkristallisation för att bringa den till rumstemperatur. Om så önskas, med lämplig stimulans, kan denna vätska tvingas att kristallisera igen. Kristallisation frigör värme och värmer upp den önskade kroppsdelen.
Industriell användning
Natriumacetat är ett alkaliskt salt som är produkten av reaktionen mellan en stark bas och en svag syra. Därför gör dess basitet, liksom dess låga kostnad, det attraktivt när det gäller att neutralisera industriella mineralsyror från urladdning.
Vid skadedjursbekämpning studeras natriumacetat för användning som en komponent i nematicider. Nematoder kan lockas till natriumacetat som bete, precis som insekter kan lockas till feromoner.


